
Onkologiekongresse
0 1 2 3 4 5
Dauer (Jahre)
Anteil
6 7 8 9 10
0
20
40
60
80
Letrozol
Placebo
100
5-Jahres-DFS:
95% LET vs. 91% PLAC
HR für DFS: 0,66; p=0,01
34%Verminderung von Rezidiven
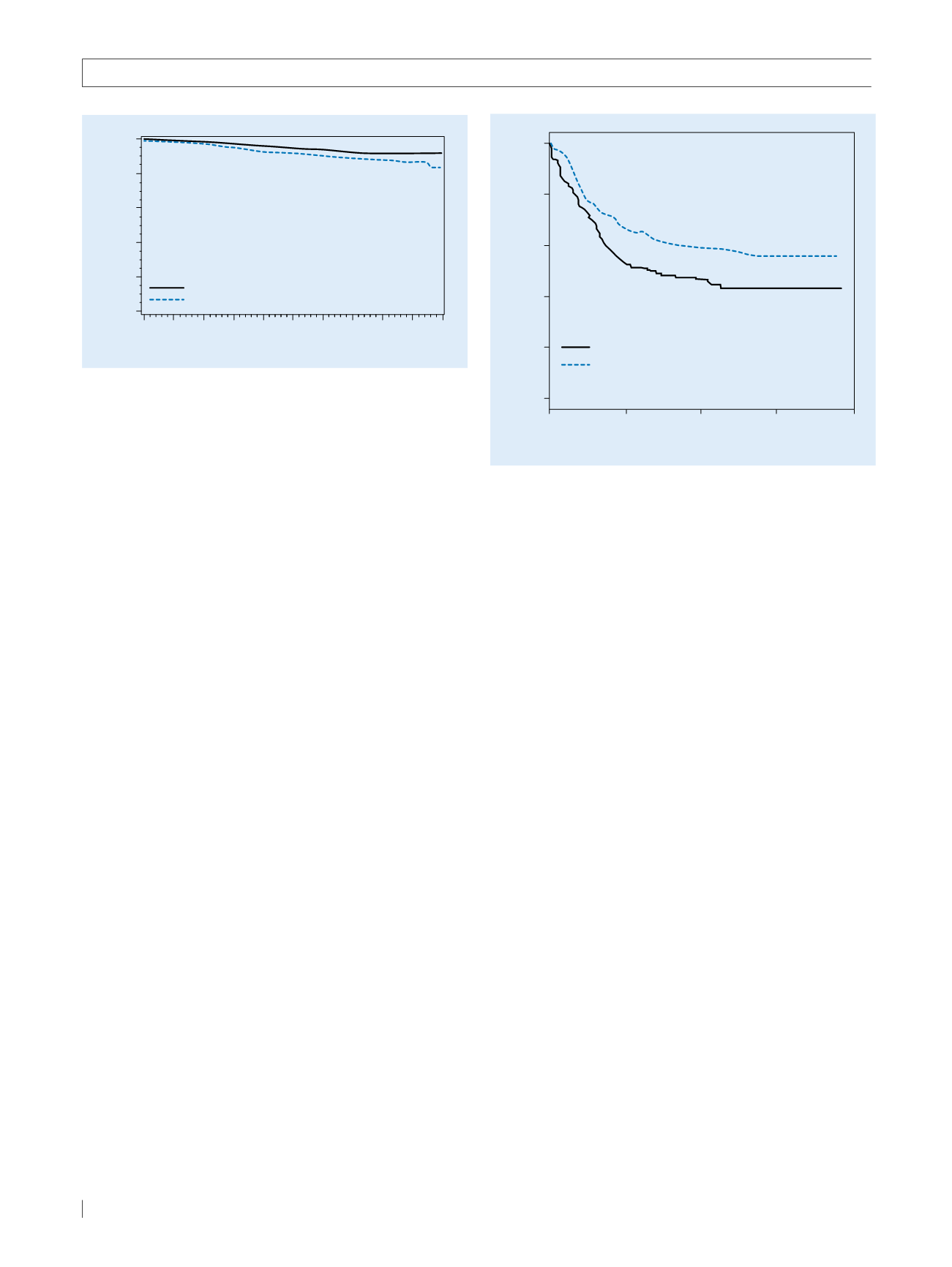
Abb. 1
8
Nach einemmedianen Follow-up von 6,3 Jahren war es für die
FrauenimLetrozol-ArmzuwenigerVorfällenundeinerstatistischsignifikant
höheren Rate an krankheitsfreiemÜberleben nach 5 Jahren gekommen.
DFS
krankheitsfreies Überleben,
LET
Letrozol,
PLAC
Placebo. (Mit freundl.
Genehmigung von P. E. Goss, ASCO 2016)
0
2
4
6
8
0,0
0,2
0,4
0,4
0,8
1,0
Einzel-ASCT
Tandem-ASCT
p
=0,008
n
=179
3-Jahres-EFS: 48,4±3,8%
Jahre nach Randomisierung
Ereignisfreie Überlebenswahrscheinlichkeit (%)
3-Jahres-EFS: 61,4±3,7%
n
=176
Abb. 2
8
Eine Tandem-Transplantation verbessert das Ereignisfreie Über-
leben für Kinder mit Hochrisiko-Neuroblastom.
ASCT
autologe Stammzell-
transplantation,
EFS
ereignisfreies Überleben. (Mit freundl. Genehmigung
von J. R. Park, ASCO 2016)
den Patienten, die TMZ erhalten hatten,
zu mehr Übelkeit, Erbrechen und Kons-
tipation als bei denen, die nur bestrahlt
worden waren.
Verbesserte Resultate durch
Chemotherapie bei seltenen
Hirntumoren
Bis zu zwei Drittel aller oligodendrog-
lialen Tumoren zeigen einen kombinier-
ten Verlust der Allele auf dem kurzen
Arm von Chromosom 1 (1p) und dem
langen Arm von Chromosom 19 (19q),
welcher wahrscheinlich auf eine Trans-
lokation zurückzuführen ist. Anaplasti-
scheOligodendrogliome, bei denen solch
einkombinierter 1p/19q-Verlust vorliegt,
sprechen besser auf eine Chemotherapie
an.
Inwieweit Patienten mit einem ana-
plastischen Gliomund ohne diesenDop-
pelverlust von1p/19q trotzdemvonTMZ
profitieren, sollte in der CATNON-Stu-
die überprüft werden
[ 4 ]. Zwischen 2007
und August 2015 wurden in diese Stu-
die 748 Patienten mit neu diagnostizier-
ten WHO-Grad-III-Gliomen und ohne
1p/19q-Verlust aufgenommen und ran-
domisiert. In der vierarmigen Studie er-
hielten alle Patienten eine Radiothera-
pie aus 59,4 Gy in 33 Fraktionen, der
Arm 1 ansonsten keine weitere Thera-
pie. Im Arm 2 erhielten die Patienten
zusätzlich zur Bestrahlung eine simulta-
ne Therapie aus täglich 75 mg/m
2
TMZ,
im Arm 3 während der Bestrahlung kei-
ne CT, dafür aber danach für 12 Monate
adjuvant TMZ. Und im Arm 4 erhiel-
ten die Patienten sowohl während der
Bestrahlung die TMZ-Therapie als auch
zusätzlichdanach für 12Monate adjuvant
TMZ. Das OS war erster Studienend-
punkt. Nach dem Auftreten von 41 %
Vorfällen war eine Interimsanalyse ge-
plant und wurde durchgeführt. Sie zeigte
eine signifikante Reduktion des Sterbe-
risikos für die Patienten, die 12 Monate
adjuvant TMZ erhalten hatten (Arme 3
und 4; HR 0,645; 95 %-KI 0,450–0,26;
p
= 0,0014). In Bezug auf das progressi-
onsfreie Überleben wurde ebenfalls das
Risiko für eine Progression durch die ad-
juvante Therapie signifikant gesenkt (HR
0,586; 95 %-KI 0,472–0,727;
p
< 0,0001).
Nacheinemnoch längerenFollow-up soll
in einer weiterenAnalyse gezeigt werden,
ob auch die TMZ-Therapie während der
Bestrahlung nützlich war.
Tandem-Transplantation für Kinder
mit Hochrisiko-Neuroblastom
Bislang lebenweniger als 20 %derKinder
mit Hochrisiko-Neuroblastomen länger
als 5 Jahre nach der Diagnose. Eine
vom NCI initiierte Studie untersuchte
nun den Nutzen einer zweiten autolo-
gen Stammzelltransplantation (ASCT)
innerhalb von 6–8 Wochen nach der
ersten. In die Phase-3-Studie wurden
652 Patienten mit neu diagnostizierten
Hochrisiko-Neuroblastomen aufgenom-
men
[ 5 ]. Alle erhielten zunächst eine
Induktionstherapie, bestehend aus 6 Zy-
klen Chemotherapie. Nach den ersten
beiden Zyklen aus hochdosiertem Cy-
clophosphamid/Topotecan (TC) erfolgte
die Stammzellernte. Nach Vollendung
der 6 Induktionszyklen wurden die
Patienten randomisiert und erhielten
dann entweder nur einmalig eine ASCT
mit Carboplatin/Etoposid/Melphalan
(CEM) oder eine Tandem-ASCT mit
Thiotepa/Cyclophosphamid vor der
ersten ASCT, gefolgt von einer mo-
difizierten CEM vor der zweiten ASCT
(TC: CEM). InderTandem-ASCT-Grup-
pe erhielten die Patienten zwei Trans-
plantationen innerhalb von 6–8Wochen.
Endpunkt der Studie war das vorfallfreie
Dreijahresüberleben (EFS).
Der Onkologe


















