
Überlebensvorteil, aber dafür mehr ko-
gnitive Defizite. Dies belegt eine Studie
(NCCTG N0574, Alliance), in der 213 Pa-
tienten mit 1 bis 3 Metastasen unter 3 cm
für Radiochirurgie allein oder zusätzliche
Ganzhirnbestrahlung randomisiert wur-
den. Drei Monate nach der Therapie wie-
sen 92% in der WBRT-Gruppe gegenüber
64% in der Gruppe mit alleiniger Radio-
chirurgie eine Abnahme kognitiver Funk-
tionen auf, speziell bezüglich des Kurz-
und Langzeitgedächtnisses und der verba-
len Flüssigkeit [12]. Deshalb hieß das Fazit
dieser Phase-III-Studie, Patientenmit we-
nigen neu aufgetretenen Metastasen nur
mit Radiochirurgie zu behandeln und
dann engmaschig zu überwachen, um die
kognitiven Funktionen zu erhalten.
Multiples Myelom
Immunonkologie
oder Proteasominhibitor?
In 2 Studien wurden sehr wirksame Kom-
binationen beim rezidivierten multiplen
Myelom vorgestellt. Die Eloquent-2-Stu-
die testete den immunstimmulierenden
Antikörper Elotuzumab. Durch Bindung
von Elotuzumab an das auf natürlichen
Killerzellen undMyelomzellen exprimier-
te „signaling lymphocytic activation mo-
lecule F7“ (SLAMF7) werden natürliche
Killerzellen stimuliert, die Myelomzellen
aber nicht. In der Studie erhielten Patien-
ten mit Rezidiv nach 1 bis 3 Vortherapien
Lenalidomid/Dexamethason allein oder
zusätzlich Elotuzumab [13]. Bei einer ge-
planten Interimsanalyse war das mediane
PFS signifikant besser im Kombinations-
arm (19,4 vs. 14,9 Monate; p<0,0004). Die
ENDEAVOR-Studie wiederum verglich
ebenfalls bei vorbehandeltem – inklusi-
ve Proteasominhibition – rezidiviertem
Myelom die beiden Proteasominhibito-
ren Carfilzomib und Bortezomib, jeweils
in Kombination mit Dexamethason [14].
Ebenfalls bei einer geplanten Interimsana-
lyse war das mediane PFS imCarfilzomib-
Arm doppelt so lang wie im Bortezomib-
Arm (18,7 vs. 9,4 Monate; p<0,0001). In
beiden Studien war das OS ein sekundä-
rer Endpunkt, aber noch nicht auswertbar.
Jeffrey Wolf, San Francisco, diskutierte
diese beiden Studien gemeinsam und be-
zog auch die Aspire-Studie [15] ein, die in
der gleichen Krankheitssituation Carfilzo-
mib/Lenalidomid/Dexamethason vs. Le-
nalidomid/Dexamethason untersuchte,
und verglich Effektivität und Kosten [16].
Wenn auch diese 3 Studien nur bedingt
vergleichbar seien, u. a. wegen nicht gleich-
mäßig verteilter Hochrisikopatienten, so
war aus seiner Sicht doch festzuhalten, dass
das PFSmit Carfilzomib/Lenalidomid/De-
xamethason am längsten war (29,6 Mona-
te [16]). Die monatlichen Kosten der Kom-
binationstherapien seien ungefähr gleich.
Da Carfilzomib eindeutig effektiver sei als
Bortezomib, stelle sich die Frage, welche
Rolle Bortezomib überhaupt noch spielen
könne. Biomarker für die Identifizierung
der individuell am besten geeigneten The-
rapie wären wünschenswert.
Last but not least – Brustkrebs
Palbociclib – längere endokrine
Therapie beim fortgeschrittenen
Mammakarzinom?
Bei ER-positivem und HER2-negati-
vem Brustkrebs bleibt nach einer Resis-
tenz gegen eine initiale Hormontherapie
100
90
80
70
60
50
40
30
20
10
0
PFS-Wahrscheinlichkeit (%)
0
2
4
6
8
10
12
Dauer (Monate)
Anzahl der Patienten mit Risiko
PAL + FUL
PCB + FUL
347
174
279
109
132
42
59
16
16
6
6
1
Medianes PFS, Monate
(95%-KI)
HR (95%-KI)
2-seitiger P-Wert
Palbociclib +
Fulvestrant
n = 347
Placebo +
Fulvestrant
n = 174
9,2
(7,5, NE)
3,8
(3,5, 5,5)
0,422 (0,318, 0,560)
<0,000001
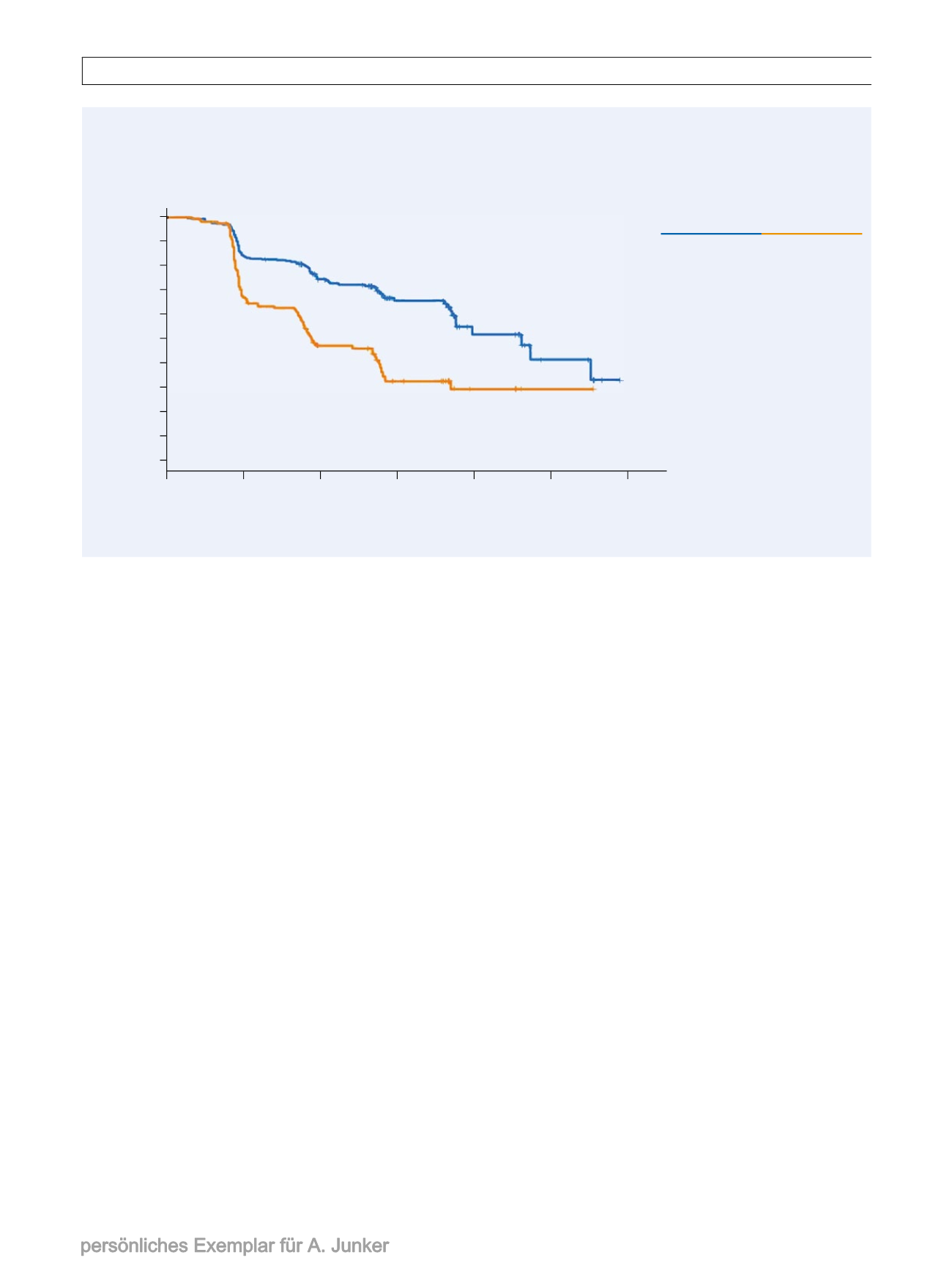
Primärer Endpunkt: PFS (ITT-Population)
Abb. 3
8
In der ITT-Population der PALOMA3-Studie lebten die Patienten mit der Palbociclib-Kombinationstherapie imMedian mehr als dop-
pelt so lang progressionsfrei wie die unter Fulvestrant-Monotherapie.
KI
Konfidenzintervall,
HR
Hazard Ratio,
ITT
Intent-to-treat-Analyse,
NE
nicht
ermittelbar,
PFS
progressionsfreies Überleben. (Aus Oral Abstract Session Breast Cancer-HER2/ER, ASCO 2015, 01.06.2015: N.C.Turner)
856 |
Der Onkologe 9 · 2015
Onkologiekongresse

















