
control
rituximab
control
104
105
63
73
45
58
34
47
months
25
35
19
26
14
18
6
10
3
5
# at risk
rituximab
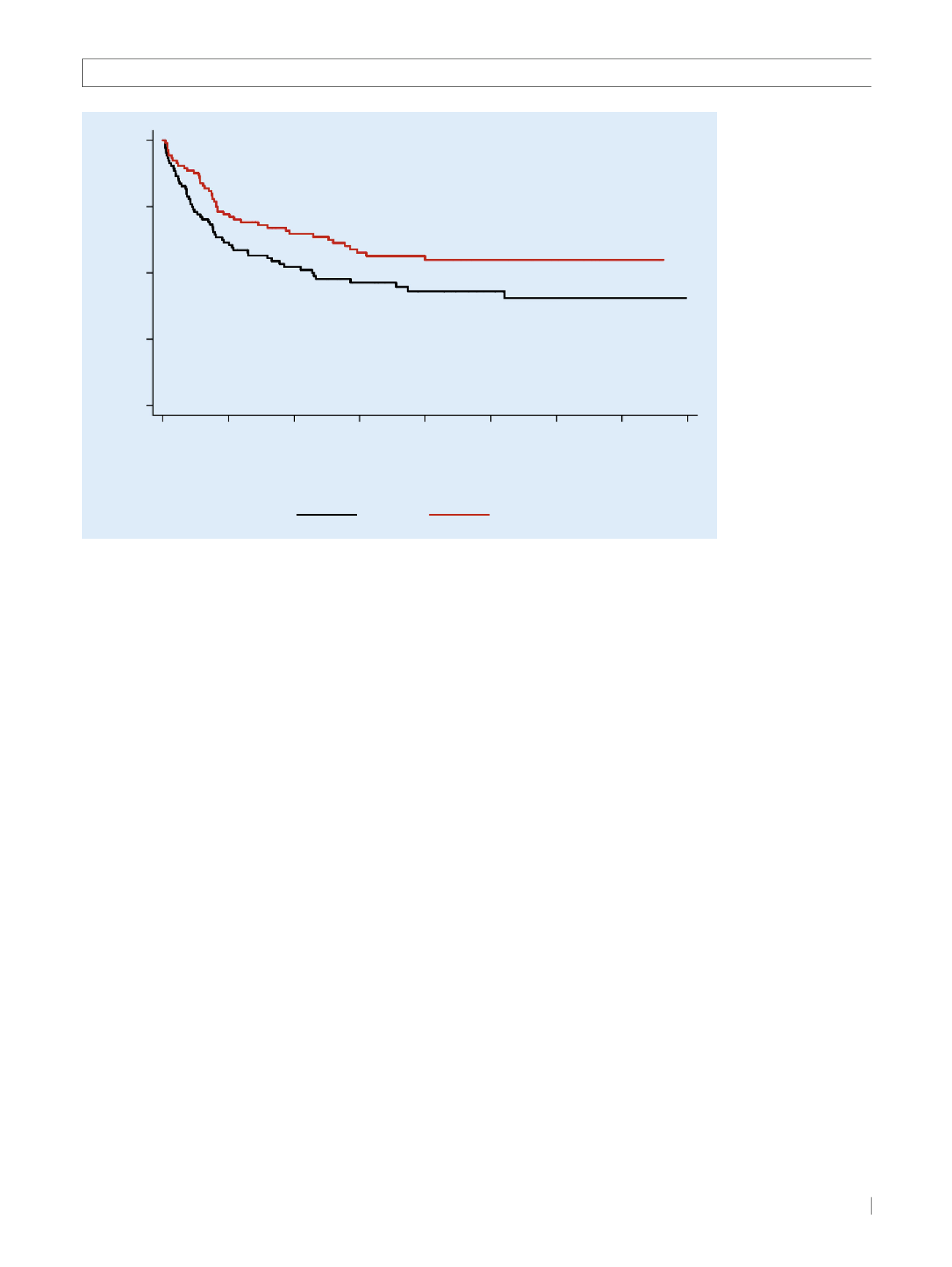
HR, 0.66 [0.45-98]
p = 0.038
0
12
24
36
48
60
72
84
96
probability of EFS
0.00
0.25
0.50
0.75
1.00
Abb. 1
9
Für die Patienten
im Rituximab-Arm ergab
sich ein signifikant längeres
ereignisfreies Überleben.
(Nach
[ 6 ])
Multiples Myelom
Einer der weltweiten Therapiestandards
für Patienten mit rezidiviertem oder re-
fraktäremmultiplemMyelom (R/RMM)
ist die Kombination aus dem Immun-
modulatorLenalidomid (Revlimid
®
)und
Dexamethason, die beide oral gegeben
werden können. Um die Wirksamkeit
zu steigern, kann ein Proteasominhibitor
zugegeben werden. Bis jetzt stehen Pro-
teasominhibitoren wie Bortezomib oder
Carfilzomibnur als intravenöse oder sub-
kutane Formulierungen zur Verfügung.
Ixazomib ist der erste oral zu applizieren-
de Vertreter dieser Klasse. Eine Phase-
3-Studie (TOURMALINE-MM1) unter-
suchte seineWirksamkeit
[ 7 ]. 722Patien-
tenmitR/RMMwurdenrandomisiertfür
Lenalidomid/Dexamethason (RD) plus
Placebo oder Ixazomib an den Tagen 1,
8 und 15 eines Zyklus (IRD) bis zum
Progress oder dem Auftreten intolera-
bler Nebenwirkungen. Zum Zeitpunkt
der ersten Interimsanalyse nach einem
medianenFollow-up von15Monatenbe-
trug das mediane PFS 20,6 vs. 14,7 Mo-
nate (IRD vs. Placebo-RD;
p
= 0,012).
Durch Ixazomib erhöhte sich die Toxi-
zität der Behandlung im Vergleich zu
RD nur geringfügig. Bei 68 % vs. 61 %
der Patienten kam es zu schweren, aber
nicht lebensbedrohlichen Nebenwirkun-
gen.VonderFDAwurde Ixazomibbereits
imNovember zugelassen. Damit steht für
R/R MM jetzt eine wirksame und aus-
schließlich orale Dreierkombination un-
ter Einschluss eines Proteasominhibitors
zur Verfügung.
Chronisch-lymphatische
Leukämie
Ibrutinib „first line“ wirksamer als
Chlorambucil
Das Arsenal an wirksamen Medikamen-
ten zur Behandlung der CLL ist mittler-
weile beträchtlich. Nach den Empfehlun-
gen der deutschen CLL-Studiengruppe
(DCLLSG) werden sie in Abhängigkeit
von Alter und Gesamtgesundheitszu-
stand des Patienten sowie vom Muta-
tionsstatus eingesetzt. Auf drei Studien
zur CLL, die mit neuen Substanzen be-
achtliche Ergebnisse ausweisen, wurde
während des ASH-Kongresses besonders
hingewiesen. Sie könnten zu Ergänzun-
gen der DCLLSG-Empfehlungen führen,
nach denen etwa der BTK-(Brutons-Ty-
rosinkinase-)Inhibitor Ibrutinib erst in
der Zweitlinientherapie oder nur bei un-
günstigem Mutationsprofil schon „first
line“ verwendet werden sollte. Eine
randomisierte Phase-3-Studie (RESO-
NATE-2) legt nun nahe, Ibrutinib be-
sonders bei älteren Patienten bereits in
der Erstlinientherapie einzusetzen
[ 8 ].
Hier wurden 269 Patienten über 65 Jah-
re (median 73 Jahre) mit zuvor noch
nicht behandelter CLL/SLL mit täglich
Ibrutinib oder mit Chlorambucil an den
Tagen 1 und 15 eines 28-tägigen Zy-
klus bis zur Progression behandelt. Nach
einemmedianenFollow-up von18,4Mo-
naten hatte Ibrutinib den Auswertungen
zufolge das Risiko für Progression oder
Tod um 91 % gesenkt (HR 0,09; 95 % CI:
0,04–0,17;
p
< 0,0001;
.
Abb.
2 ). Nach
zwei Jahren lebten noch 97,8 % im Ibru-
tinib- vs. 85,3 % im Chlorambucil-Arm.
Insgesamt zeigen 90,4 % vs. 35,3 % der
Patienten ein Therapieansprechen. Die
mediane Behandlungsdauer betrug 17,4
vs. 7,1 Monate für Ibrutinib vs. Chlo-
rambucil. Ibrutinib verbesserte auch sig-
nifikant die Knochenmarkfunktion mit
anhaltendem Anstieg des Hb-Werts und
derThrombozytenzahlen. An Nebenwir-
kungen traten unter Ibrutinib am häu-
figsten (
≥
20 %) Diarrhö, Fatigue, Husten
und Übelkeit auf, unter Chlorambucil
Übelkeit, Fatigue, Neutropenie, Anämie
und Erbrechen. Therapieabbrüche auf-
grund der Nebenwirkungen waren im
Ibrutinib-Arm seltener (9 % vs. 23 %).
Der Onkologe 3 · 2016
209


















