
nicht bestätigt [(]. In mehr als +#* der
Fälle sind Patienten mit NSCLC Stadium
I durch alleinige Operation effektiv und
ausreichend behandelt. In $–'* der Fäl-
le kommt es allerdings zu einemZweittu-
mor im ersten Jahr nach der Operation.
In einer randomisierten, doppelblinden
Phase-III-Studie erhielten $&'' Patienten
mit NSCLC der Stadien IA und IB nach
der Operation entweder für % Jahre Selen
('## µg/Tag) oder Placebo. Nach medi-
an etwas mehr als vier Jahren wurde die
Studie allerdings abgebrochen, weil sich
gezeigt hatte, dass in der Placebogrup-
pe "+*, in der Selengruppe dagegen nur
"'* der Patienten progressionsfrei über-
lebt hatten (p=#,$&). Einen Zweittumor
hatten $,,* in der Selen- und $,%* in der
Placebogruppe entwickelt.
Chronische myeloische
Leukämie (CML) in der
chronischen Phase: Die Ära nach
Imatinib wird eingeläutet
Imatinib hat seine Effektivität und Über-
legenheit gegenüber den vorher zur Ver-
fügung stehenden Therapieoptionen bei
CML nachhaltig durch die eindrucksvol-
le Verbesserung der Behandlungsergeb-
nisse bewiesen:
F
Im Jahr '##$ erkrankten ca. %"## Pa-
tienten neu an CML, '(## starben
daran.
F
Im Jahr '#$# erkrankten ca. %+"# Pa-
tienten, und nur %%# starben dadurch.
Bei ungefähr einem Drittel der neu di-
agnostizierten CML-Patienten, die mit
dem BCR-ABL-Tyroskinaseinhibitor
Imatinib behandelt werden, kommt es
allerdings nach $' Monaten nicht zu ei-
ner kompletten zytogenetischen Remis-
sion (CCyR) mit Verschwinden des Phi-
ladelphia-Chromosoms, sie entwickeln
eine Resistenz gegen Imatinib und ha-
ben ein erhöhtes Progressionsrisiko. Die
CCyR ist ein guter Surrogatparameter
für das Langzeitüberleben von CML-Pa-
tienten. Die beiden Tyrosinkinaseinhibi-
toren (TKI) der zweiten Generation, Ni-
lotinib und Dasatinib, sind in den meis-
ten Fällen von Imatinibresistenz wirk-
sam und für die Zweitlinientherapie zu-
gelassen. Außerdem können sie bei Ima-
tinibunverträglichkeit eingesetzt werden.
Zwei auf der Tagung vorgestellte Phase-
III-Studien prüften Nilotinib bzw. Dasa-
tinib in der First-Line-Therapie der CML
im Vergleich zu Imatinib. In der einen
Studie wurde bei +%) Patienten Niloti-
nib in ' Dosierungen ((## oder %## mg
pro Tag) mit Imatinib %# mg täglich) ver-
glichen [%]. Primärer Endpunkt war das
molekulare Ansprechen (MMR: ≤#,$*
BCR-ABL) nach $' Monaten. Die MMR-
Rate betrug nach $ Jahr %%* bzw. %(* in
den beiden Nilotinibarmen vs. ''* im
Imatinibarm. Die $+-Monatsdaten bestä-
tigten die positiven Ergebnisse. Damit
zeigt Nilotinib ein besseres molekulares
Ansprechen als Imatinib mit entspre-
chend geringerem Progressionsrisiko. In
der zweiten Studie [&] erhielten &$, unvor-
behandelte Patienten entweder Dasatinib
($## mg täglich) oder wiederum %## mg
Imatinib. Primärer Endpunkt war hier
das bestätigte zytologische Ansprechen
(CCyR) nach $' Monaten, das unter Da-
satinib ""*, unter Imatinib nur ))* be-
trug (p=#,##)"). Solange noch keine ge-
eigneten Screening-Tools zur Prädiktion
des Ansprechens auf Imatinib zur Verfü-
gung stehen, sollten nach Auffassung von
Michael Mauro, Portland, der die Beiträge
diskutierte, die Zweitgenerations-TKI pri-
mär eingesetzt werden – ihre Zulassung
für die Erstlinientherapie vorausgesetzt.
Welche Substanz besser und nachhaltiger
wirksam ist, werde sich erst nach länge-
rer Beobachtung der Dauer des progres-
sionsfreien Intervalls im Vergleich zei-
gen. Die Patienten, die bereits auf Imati-
nib eingestellt seien, sollten allerdings bei
gutemAnsprechen und guter Verträglich-
keit auch damit weiter behandelt werden.
Eine Umstellung auf einen Zweitgenerati-
on-TKI solle hier erst bei Unverträglich-
keit oder Progression erfolgen.
Metastasierte Melanome:
Antikörper verlängert
das Überleben
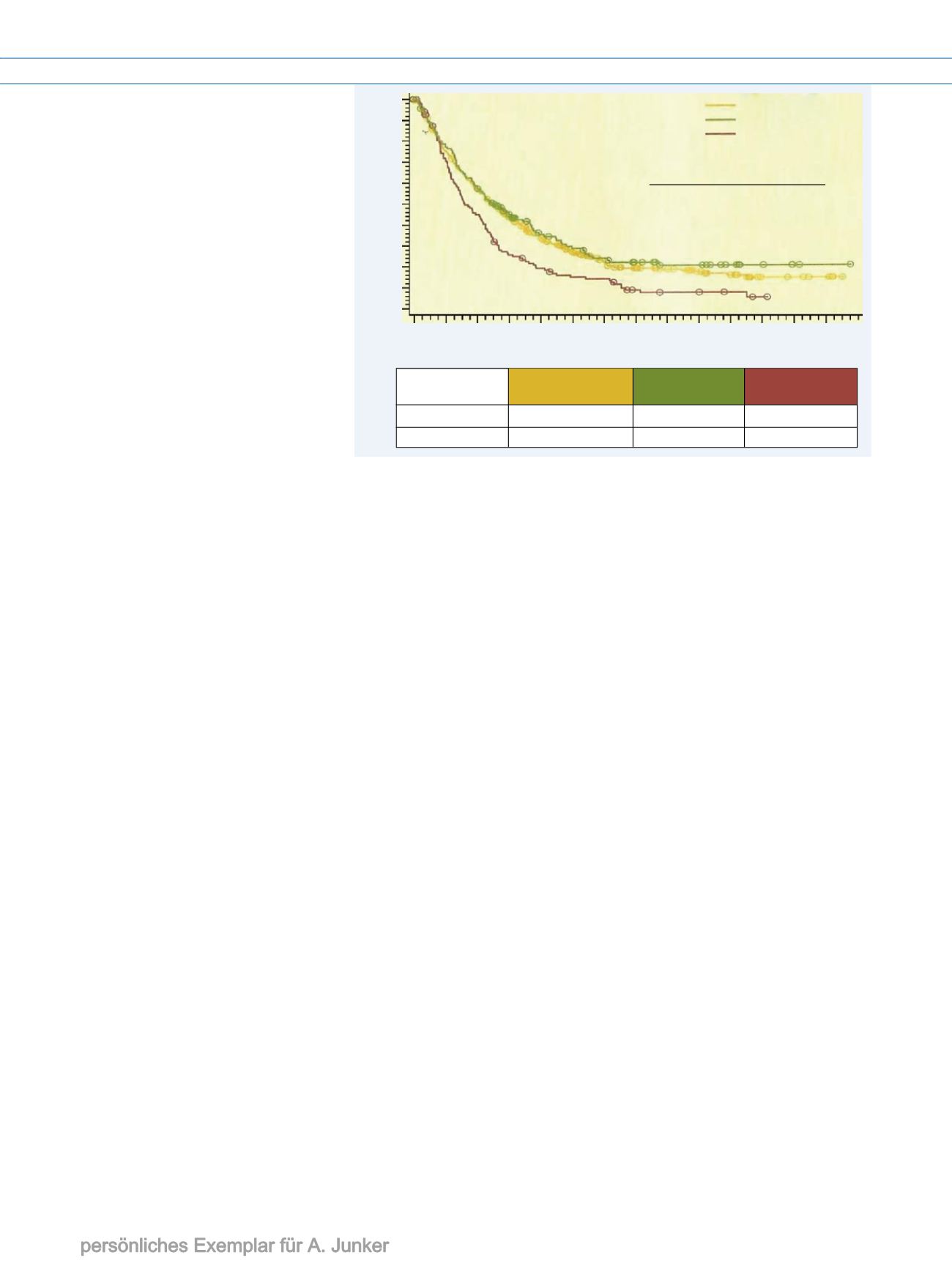
In einer Phase-III-Studie erreichte der
neue Antikörper Ipilimumab bei Patien-
ten mit fortgeschrittenen, vorbehandel-
ten Melanomen deutlich höhere Überle-
bensraten als eine gp$##-Peptid-Vakzine
(
.
Abb. 1,
[)]). In einer Situation, in der
nur wenige Therapieoptionen zur Verfü-
gung stehen, konnte erstmals ein Über-
lebensbenefit gezeigt werden, resümier-
te Studienleiter Steven O’Day, Los An-
geles. Ipilimumab ist ein monoklonaler
Antikörper zur parenteralen Applikati-
on, der T-Zellen des Immunsystems ge-
gen Melanomzellen aktiviert. Die dreiar-
mige multizentrische Studie verglich bei
knapp "## Patienten Ipilimumab plus
Placebo, Ipilimumab plus gp$##-Vak-
zine und gp$##-Vakzine plus Placebo.
Die Vakzine, die ebenfalls T-Zellen sti-
muliert, war in vorausgegangenen Studi-
Anteil Überlebender
1,0
0,9
0,8
0,7
0,6
0,5
0,4
0,3
0,2
0,1
0
1
Überlebensrate
1 Jahr
44%
22%
24%
46%
25%
14%
Jahre
Ipi + gp100 (A)
Nur Ipi (B)
Nur gp100 (C)
Vergleich
A vs. C
0,68 0,0004
0,0026
0,66
B vs. C
HR p-Wert
2 Jahre
Ipi + gp100
403 Patienten
Ipi + Placebo
137 Patienten
gp100 + Placebo
136 Patienten
2
3
4
Abb. 1
8
Anteil Überlebender.
HR
Hazard Ratio,
Ipi
Ipilimumab,
gp100
gp100-Vakzine,
KI
Konfidenzin-
tervall
805
Der Onkologe 8 · 2010
|

















