
Grad I und II, ebenso Anämie, die aber
nur in weniger als *% Grad + erreichte.
Auch bei Mantelzelllymphomen [+]
sowie diffus großzelligen Lymphomen [*]
zeigte Ibrutinib hohe Ansprechraten bei
guter Verträglichkeit.
Wenn sich diese Resultate auch in Pha-
se-III-Studien bestätigen lassen, könnte
der schlechte Ruf von !(p- und !!q-De-
letionen der Vergangenheit angehören.
Aufgrund dieses deutlichen und dauer-
haften Ansprechens auch bei Patienten
mit weit fortgeschrittener Erkrankung ti-
tulierten Optimisten Ibrutinib bereits als
„das Imatinib der CLL“.
Multiples Myelom:
Überlebensvorteil mit
Pomalidomid
Für Patienten mit stark vorbehandeltem
und refraktärem multiplem Myelom gibt
es kaum wirksame Behandlungsoptio-
nen. Verschiedene Kombinationen mit
Dexamethason als Entzündungshemmer
oder Dexamethason allein und hoch do-
siert werden eingesetzt; eine Standardthe-
rapie gibt es nicht. Entsprechend führte
eine multizentrisch durchgeführte Phase-
III-Studie (MM-$$') mit dem neuen Im-
munmodulator Pomalidomid (POM) zu
besonderer Aufmerksamkeit, zumal eine
signifikante Verlängerung von progres-
sionsfreiem und Gesamtüberleben ge-
zeigt werden konnte. Zielkriterien waren
Sicherheit und Wirksamkeit der Kombi-
nation von Pomalidomid und niedrig do-
siertem Dexamethason (LoDEX) [%]
Die in die Studie eingeschlossenen +**
rezidivierten oder refraktären Patienten
hattenmedian * Vortherapien (! bis !() er-
halten. Sie wurden &:! randomisiert: Po-
malidomid (Tage !–&!) plus Dexametha-
son +$ mg (Tage !, #, !* und &&; POM/Lo-
DEX; ArmA) oder Dexamethason +$ mg
(Tage !–+, "–!& und !(–&$; Hi-DEX; Arm
B). Patienten über (* Jahre erhielten in
beiden Armen nur &$ mg Dexamethason.
Die Behandlung wurde bis zum Progress
oder inakzeptabler Toxizität fortgeführt.
Patienten imHi-DEX-Arm konnten nach
Progress Pomalidomid erhalten [%]. Nach
einem medianen Follow-up von !# Wo-
chen betrug das mediane progressions-
freie Überleben im Arm A !*,( vs. # Wo-
chen imArm B (HR=$,+*; p<$,$$!). Auch
die Interimsanalyse zum Gesamtüberle-
ben (OS) zeigte einen signifikanten Vor-
teil für die Kombination. Der Median war
hier noch nicht erreicht. ImHi-DEX-Arm
betrug es '+ Wochen (p<$,$$!). Signifi-
kant höher war auch die Gesamtansprech-
rate in Arm A (!%,%% vs. ',"%; p<$,$$!).
Unter Einbeziehung der Krankheitsstabi-
lisierungen ergab sich für die Therapiemit
Pomalidomid/Dexamethason in (#,!% vs.
*%,"% ein deutlicherer klinischer Nutzen.
Studienleiter Melethios Dimopoulos,
Athen, plädierte dafür, diese Behandlung
auch in früheren Therapielinien oder be-
reits „first line“ zu prüfen.
Situation verbessern für
Patientenmit erhöhtemRisiko
für Thromboembolien
Patienten mit Polycythämia vera (PV)
haben aufgrund der erhöhten Zellzahl im
Blut ein erhöhtes Risiko für thromboem-
bolische Komplikationen. Ihr Hämatokrit
ist ebenfalls erhöht. Den Resultaten einer
in Atlanta vorgestellten Studie zufolge ist
der Hämatokrit während einer PV-The-
rapie ein sinnvolles Zielkriterium: Ein
Hämatokrit zwischen +*% und *$% ist
demnach im Vergleich zu Werten unter
+*% mit einem +-fach höheren Risiko für
schwerwiegende thromboembolische Er-
eignisse verbunden [(].
Ungefähr bei einemDrittel der Patien-
ten, die schon einmal ein venöses throm-
boembolisches Ereignis (VTE) hatten,
kommt es innerhalb der folgenden !$ Jah-
re erneut zu einem solchen. Als derzeit
übliche Behandlungen stehen antikoagu-
lierende Substanzen wie Warfarin, Phen-
procoumon, Dabigatran und Rivaroxa-
ban zur Verfügung. Diese beugen zwar
Thrombosen wirksam vor, aber eine re-
gelmäßige Blutkontrolle und Dosisanpas-
sung ist erforderlich, und trotzdem be-
steht das Risiko von Blutungen.
Möglicherweise kann Apixaban hier
Abhilfe schaffen, da es anders als die er-
wähnten Medikamente nur den aktivier-
ten Faktor X hemmt. Im Gegensatz zu
Warfarin kann Apixaban in fixen Do-
sen appliziert werden. In einer dreiarmi-
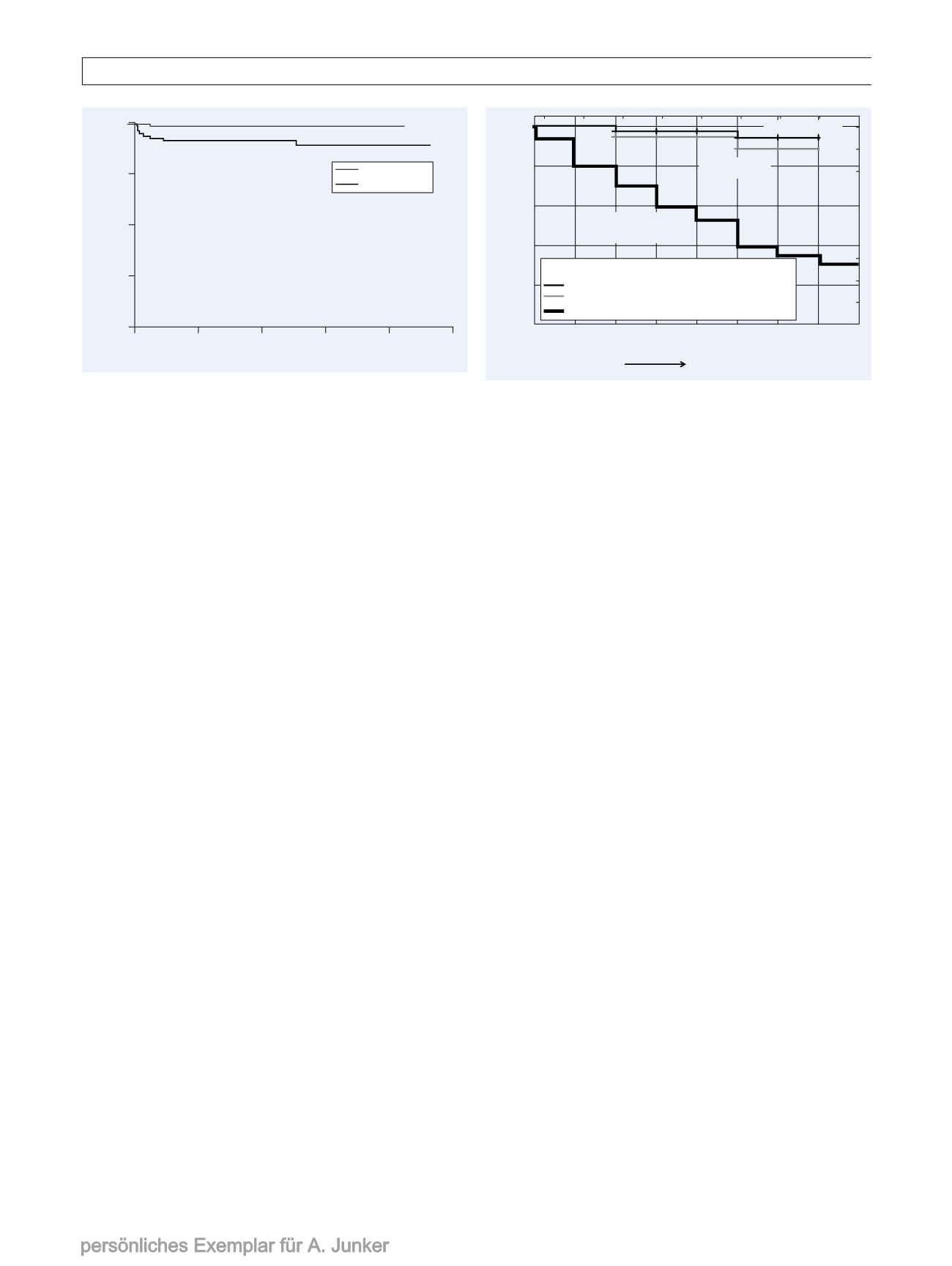
98,7%
91,1%
p=0,02
ATRA-ATO
ATRA-Chemo
Gesamtüberlebenswahrscheinlichkeit
Monate seit Diagnose
100
75
50
25
0
0
12
24
36
48
60
Abb. 1
8
APL 0406 – Gesamtüberleben. Das Gesamtüberleben bei APL-
Patienten ist unter einer Therapie mit ATO plus ATRA signifikant länger als
unter ATRA plus Chemotherapie [1].
ATRA
All-trans-Retinsäure,
ATO
Arsentrioxid
Anteil Therapieversager
Zeit (Monate)
1,0
0,8
0,6
0,4
0,2
0,0
0
1
2
3
4
5
6
7
8
Del17p mit
üblicher Salvage-Therapie
Alle Pat. mit IR
Del17p mit IR
Ibrutinib + Rituximab (alle Pat.)
Ibrutinib + Rituximab (nur 17p )
Chemotherapie (1/p-Salvage-Pat.)
Pat. Versager Therapie
40
20
122
2
2
8/
Abb. 2
8
Zeit bis zumTherapieversagen unter der Therapie mit Ibrutinib
plus Rituximab imVergleich zu einer bisher üblichen Chemo-/Immunthera-
pie bei vorbehandelten Patienten mit 17p-Mutation [3].
IR
Rituximab,
Pat.
Patienten
320 |
Der Onkologe 4 · 2013
Onkologiekongresse

















